Элементарный состав твердого и жидкого топлив.
По техническим характеристикам твердое и жидкое топлива представляют собой комплекс сложных органических и минеральных соединений и состоят из горючей и негорючей частей.
Молекулярная и химическая структура горючей части изучена не достаточно полно и до настоящего времени не поддается подробной расшифровке. Вследствие этого химический состав горючей части выявить (т. е. определить вид и формулу химических соединений) чрезвычайно сложно. Структура и химические соединения, входящие в негорючую часть, наоборот, исследованы достаточно подробно.
Органическое твердое и жидкое топлива характеризуются элементарным составом, который условно представляют как сумму всех химических элементов и соединений, входящих в топливо. При этом их содержание дается в процентах к массе 1 кг топлива. Элементарный состав не дает представления о молекулярной и химической структуре топлива. Для твердого и жидкого топлив элементарный состав можно записать в следующем виде:
C + H + Sл + O + N + A + W = 100%.(18.1)
В горючую часть топлива входят углерод, водород и сера(летучая). Летучая сера Sл - это сера, входящая в состав органических соединений и серного колчедана FeS2, т. е.
Sл = Sорг + Sк (18.2)
где Sк принято называть колчеданной серой.
Следует отметить, что летучая сера, входящая в горючую часть топлива, является только частью общего содержания серы. Другую часть составляет сера, входящая в минеральные соли (CaSО4, MgSО4, FeSО4 и др.). Сера, содержащаяся в минеральных солях, называется сульфатной Sc. Следовательно,
Sобщ = Sл + Sc (18.3)
В негорючую часть топлива входят азот N, кислород О, влага W, минеральные негорючие вещества, которые после сжигания топлива образуют золовый остаток А.
При изучении технических характеристик твердого и жидкого топлив различают их рабочую, сухую, горючую и органическую массы. Составу каждой массы присваивается соответствующий индекс: рабочей - р, сухой - с, горючей - г и органической - о.
Топливо в том виде, в каком оно поступает к потребителю и подвергается сжиганию, называется рабочим, а масса и ее элементарный состав - соответственно рабочей массой и рабочим составом.
Элементарный состав рабочей массы записывают следующим образом:
Cp + Hp + Sp/л + Op + Np + Ap + Wр = 100 % (18.4)
Негорючие элементы в технических характеристиках топлива составляют его балласт, при этом кислород и азот принято называть внутренним балластом топлива, а золу и влагу - внешним, поскольку их содержание в значительной степени зависит от таких внешних факторов, как способы добычи и хранения топлива.
В рабочий состав отдельных видов топлива некоторые элементы могут и не входить, например в дровах отсутствует летучая сера.
Сухая масса топлива в отличие от рабочей массы не содержит влаги и может быть представлена равенством:
Сс + Hc + Sс/л + Oc + Nc + Ас = 100 %. (18.5)
Формулы пересчета с рабочей массы на сухую имеют вид:
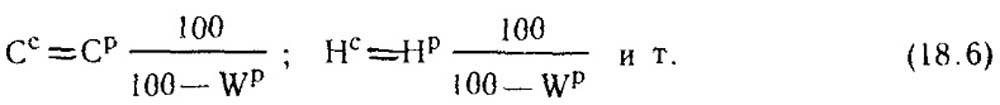
Зольность топлива всегда проверяется только по сухой массе топлива.
Горючий состав топлива не содержит внешнего балласта, т. е. влаги и золы, и может быть записан так:
Сг + Hr + Sr/л + Or + Nr = 100%(18.7)
Название "горючая масса" - условное, так как действительно горючими ее элементами являются только С, Н и S состав горючей массы ископаемого топлива зависит от характера и условий происхождения топлива, а также от его геологического возраста (т. е. глубины происшедших необратимых превращений в органических веществах).
Содержание углерода в твердом топливе растет с его геологическим возрастом, а содержание водорода уменьшается. Так, например, содержание углерода в торфе составляет Сг = 50 ÷ 60 %, в буром угле Сг = 60 ÷ 75 %, в каменном угле Сг = 75 ÷ 90 %. С уменьшением геологического возраста содержание растительных остатков в топливе увеличивается.
Пересчет с сухой и рабочей масс топлива на горючую производят по формуле
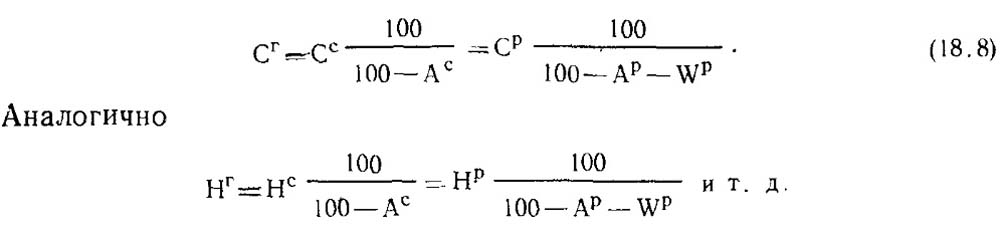
Органическая масса топлива в отличие от горючей содержит только органическую серу и не включает колчеданную. Состав этой массы может быть выражен равенством:
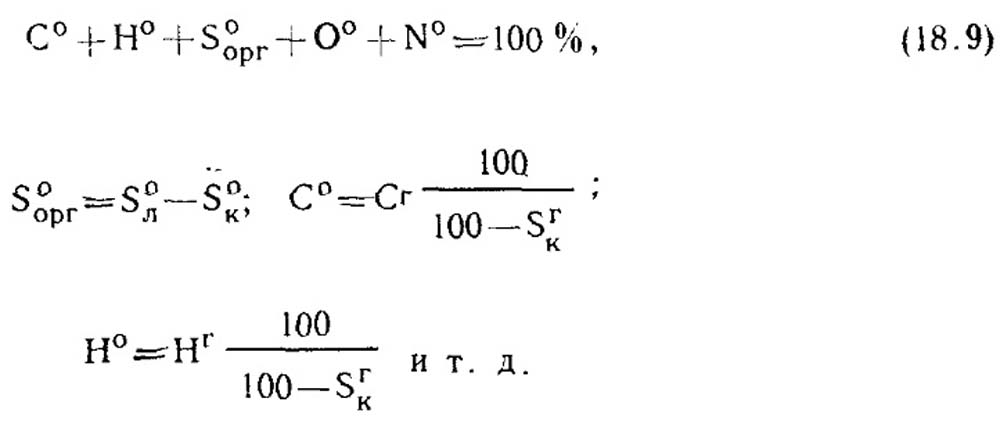
Во всех теплотехнических расчетах состав топлива берется по его рабочей массе, являющейся наиболее полной характеристикой состояния топлива перед его сжиганием.
Технические характеристики топлива: влажность топлива.
В зависимости от способа добычи, транспортировки, хранения и т. п. количество влаги Wp может колебаться для одного и того же сорта топлива в больших пределах. Средняя влажность топлива в рабочем состоянии составляет, %: для торфа 50, сланцев 13 - 17, каменного угля 5 -14 и антрацита 5 - 8. Бурые угли в зависимости от влажности делят на три группы: группу Б1 с Wp >40%, группу Б2 с содержанием влаги Wp = 30 ÷ 40 % и группу Б3 с влажностью Wp ≤ 30 %. Общее содержание влаги в топливе включает внешнюю, или воздушную WBH, и внутреннюю, или гигроскопическую Wгиг влагу. Первый вид влаги определяют, просушивая топливо при комнатной температуре до постоянной массы, а второй вид - лабораторным путем, просушивая пробы топлива при 378 К. Гигроскопическая влажность топлива зависит от его структуры: чем больше пористость, тем больше Wгиг. Средняя гигроскопическая влажность топлива составляет, %: для торфа 10, древесины 7, бурых углей 6 - 10, каменных углей 1 - 5 и антрацита 2 - 3. Наличие влаги в топливе нежелательно не только потому, что из - за этого уменьшается доля горючих компонентов в единице массы топлива, но и потому, что она снижает тепловой эффект горения, отнимая часть теплоты на испарение.
Зола топлива. Присутствие в топливе золы нежелательно, так как вследствие ее наличия уменьшается количество теплоты, выделяющейся при сгорании, возникает эрозия металлических частей оборудования и ухудшается экономичность работы топочных устройств. Количество золы определяют по остатку от прокаливания сухого топлива в атмосферном воздухе при 1070 К. В состав золы входят преимущественно соли щелочных и щелочно - земельных металлов, окислы железа, алюминия, а также сульфатная сера. Наиболее сложный состав у сланцевой золы, в которую помимо упомянутых соединений входит большое количество карбонатных соединений: CaCО3, MgCО3, окись кремния, алюмосиликаты и т. д.
При нагревании сланцевой золы карбонатные соединения разлагаются с выделением свободной двуокиси углерода СОк/2. Вследствие этого видимая масса золы получается меньше действительной ее массы в топливе. Зольность сланцев определяют по специальной методике.
Минеральные остатки, образующиеся после сгорания топлива, имеют вид либо сыпучей массы (зола), либо сплавленных кусков (шлак). При высоких температурах, развивающихся при горении топлива, зола размягчается, а затем плавится. Размягченные зола и шлак прилипают к стенкам обмуровки топки, уменьшают сечение газоходов, откладываются на поверхностях нагрева, увеличивая тем самым термическое сопротивление в процессе теплопередачи от газов к нагреваемой среде, забивают отверстия для прохода воздуха в колосниковой решетке, обволакивают частицы топлива, затрудняя их сжигание. Зола с температурой плавления ниже 1470 К считается легкоплавкой, выше 1720 К - тугоплавкой. Плавкость золы зависит от ее химического состава. Зола древесного топлива не шлакуется, а торф имеет легко шлакующуюся золу.
Различные виды топлива содержат золу в широко колеблющемся количестве. Например, средняя зольность сухой массы топлива Ас составляет, %: для древесины 1, торфа 10, кузнецкого угля 10 - 20, подмосковного бурого угля 30, сланцев 60. Бурые угли и сланцы относятся к многозольным видам топлива. Жидкое топливо (мазут) также включает небольшое количество (0,2 - 1%) минеральных примесей, попадающих в топливо с растворами различных солей из буровых вод и при коррозии труб, цистерн и нефтехранилищ.
Летучие вещества и кокс. Из твердого топлива, нагретого до температуры 870 - 1070 К без доступа окислителя, выделяются парогазообразные вещества, которые называются летучими. Летучие вещества представляют собой продукты распада сложных органических веществ, содержащихся в органической массе топлива. В состав летучих веществ входят молекулярный азот N2, кислород О2, водород Н2, окись углерода СО, углеводородные газы СН4, С2Н4 и т . д., а также водяные пары, образующиеся из влаги, содержащейся в топливе.
Химический состав летучих веществ зависит от условий процесса нагревания топлива. Сумма летучих веществ обозначается Vr и относится только к горючей массе.
Содержание летучих веществ в ископаемом твердом топливе колеблется в широких пределах. Наиболее богаты по выходу летучих веществ сланцы (Vr = 90 %), торф (Vr = 75 %). Выход летучих веществ у бурых углей достигает 40 - 50 %, а у антрацитов - 4 - 6 %.
Твердый остаток, который получается после нагревания топлива (без доступа окислителя) и выхода летучих, называется коксом. В состав кокса входят остаточный углерод и зола. В зависимости от условий нагревания (например, при низких температурах) в твердом остатке кроме золы может оказаться часть элементов (С, N, Sл, Н), входящих в состав сложных органических соединений, для термического разложения которых требуется более высокая температура. В этом случае твердый остаток называется полукоксом.
По своим механическим свойствам твердый остаток (кокс) может быть порошкообразным, слабоспекшимся и спекшимся. Свойство некоторых углей (коксующихся) давать спекшийся, механически прочный кокс используется для получения металлургического кокса, применяемого в доменном процессе.
В зависимости от выхода летучих веществ и характеристики кокса каменные угли разделяются на 10 марок: длиннопламенный Д, газовый Г, газовый жирный ГЖ, жирный Ж, коксовый жирный КЖ, коксовый К, коксовый второй к2, отощенный спекающийся ОС, слабоспекающийся СС, тощий Т.
Каменные угли с выходом летучих Vr - 174 - 37 % относятся к марке СС. При Vr = 254 - 37 % эти угли относятся к первому классу (1СС), а угли с Vr = 17 ÷ 25 % - ко второму (2СС).
В настоящее время ископаемые угли классифицируют также в зависимости от крупности кусков: крупный К (размер 50 - 100 мм), орех О (25 - 50 мм), мелкий М (13 - 25 мм), семечко С (6 - 13 мм), штыб Ш (< 6 мм), рядовой Р (размер не ограничен, т. е. топливо не отсортировано).
Пример расшифровки марки и класса углей: ДР - длиннопламенный рядовой; ПАР - полуантрацит рядовой; БlР - бурый уголь класса 1, рядовой и т. д. (табл. 18.2).
Жидкое топливо. Нефть является основным источником получения искусственных жидких топлив. В процессе сухой перегонки углей и горючих сланцев также получаются некоторые виды жидких топлив. В топках котельных агрегатов и технологических печей используется в основном мазут - остаточный продукт переработки нефти. В состав мазута входят углерод, водород, сера, кислород, азот.
Основными характеристиками мазута являются вязкость и температура застывания. Применяется топочный мазут трех марок; №40, №100, №200. Марка мазута определяется предельной вязкостью при 353 К. По содержанию серы мазуты делятся на малосернистые (до 0,5 %), сернистые (до 2 %) и высокосернистые (3,5 - 4,3 %).
Газообразное топливо представляет собой смесь горючих, и негорючих газов. Горючая часть газообразного топлива состоит из предельных (CnH2n + 2) и непредельных (СnН2п) углеводородов, водорода, окиси углерода и сернистого водорода (H2S). В состав негорючей части входят азот, углекислый газ и кислород. Количество водяных паров в газе обозначается d и задается обычно в кг/м3.
Таблица 18.2. Основные характеристики твердого и жидкого топлива
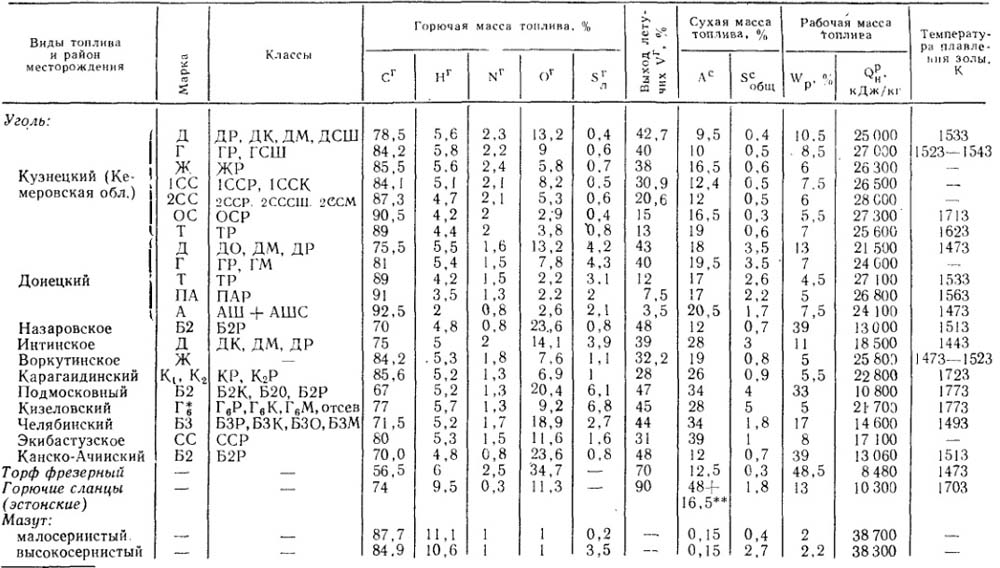
Таблица 18.3. Основные характеристики горючих газов
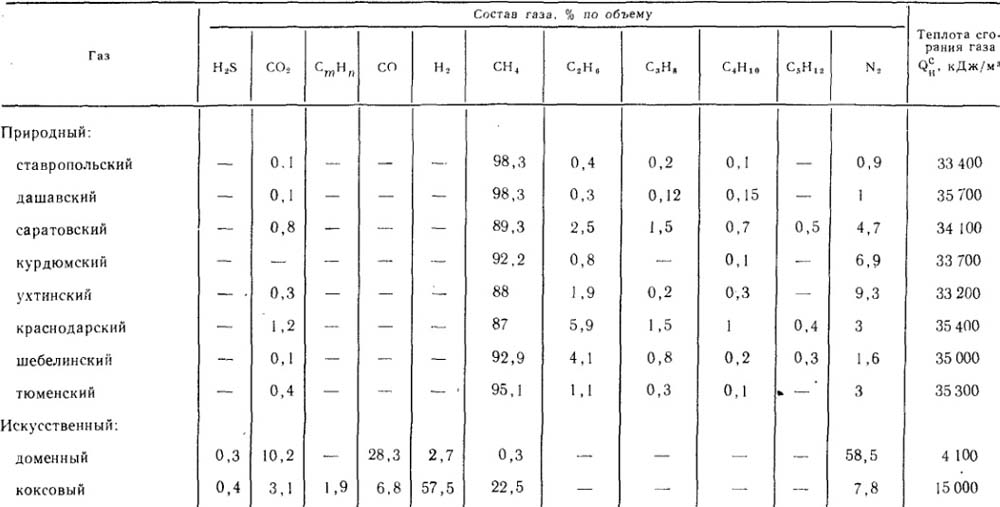
Составы природного и искусственного газообразных топлив различны. Природный газ чисто газовых месторождений характеризуется высоким содержанием угле - водородов, в основном метана СН4 (до 98 %). В состав природного газа в небольших количествах входят другие углеводороды: этан С2Н6, пропан С3Н8, бутан, С4Н10, этилен С2Н4 и пропилен С3Н6 (табл. 18.3). Содержание балласта O2 и N2, как правило, в природном газе невелико. В так называемом попутном газе, который добывают на нефтегазовых месторождениях, наблюдается несколько повышенное содержание высших углеводородов: этана, пропана, бутана, пентана, этилена. В искусственных газах содержание горючих составляющих (в основном водорода и окиси углерода) достигает 25 - 45 %. В балласте преобладают азот и углекислота (75 - 55 %).
Состав газообразного топлива задается в объемных долях, так как количественное содержание и химические формулы компонентов определяются достаточно точно с помощью химического или хромато графического анализов.
В общем виде состав газообразного топлива можно записать следующим образом:
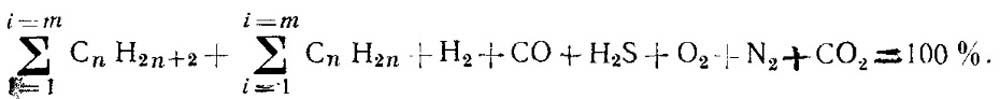
Для влажного газа объемный состав, %, определяют по формуле:
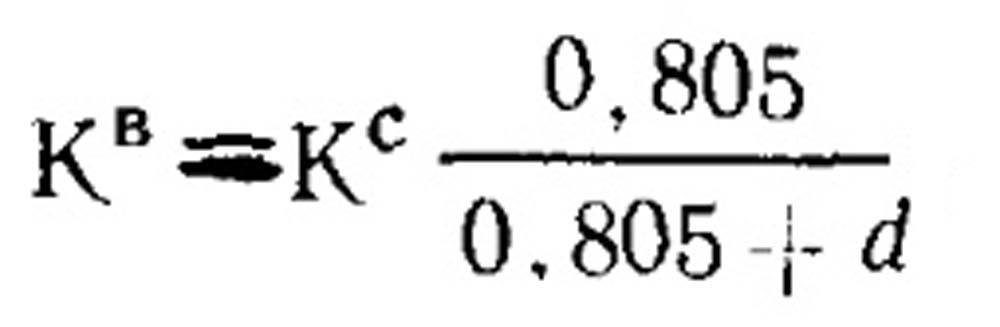
где Кв - объемное содержание компонента влажного газа: Кс - объемное содержание компонента в сухом газе; 0,805 - плотность водяного пара при нормальных условиях, кг/м3; d - влагосодержание газа, кг/м3.
Теплотехнические расчеты ведутся обычно для сухого состава топлива.
Многие физико - химические свойства и теплотехнические характеристики газового топлива и продуктов его сгорания можно установить по так называемому углеродному числу n. Сущность этого метода заключается в том, что реальная смесь углеводородов метанового ряда СnН2n+2 заменяется одним условным углеводородом, свойства которого отождествляются со свойствами смеси. Число n показывает количество атомов углерода в этом условном углеводороде (для чистого метана n = 1). Оно может быть дробным и в общем случае больше единицы. Достоинства этого метода заключаются в том, что для расчетов состава газа не требуется полный анализ его органической части. Для этого необходимо знать только количество углеводородов метанового ряда (в процентах по объему). Число n находят по формуле:
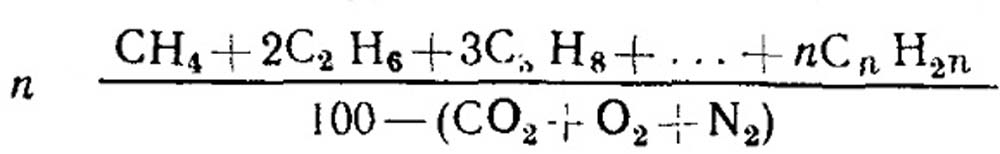 (18.11)
(18.11)
Более подробно применение этого метода изложено в специальной литературе.
Теплота сгорания. Одной из основных характеристик любого вида топлива является теплота сгорания этого топлива, т. е. то количество теплоты, которое может быть получено при полном сгорании единицы массы или объема топлива. Полным сгоранием называется такое, при котором горючие компоненты топлива С, Н и S полностью окисляются кислородом. Теплоту сгорания твердого и жидкого топлив относят к 1 кг, а газового - к 1 м3 при нормальных условиях.
Различают теплоту сгорания топлива высшую QB и низшую Qn. Различие между ними состоит в том, что в высшую теплоту сгорания топлива входит количество теплоты, которое может быть выделено при конденсации водяных паров, находящихся в продуктах сгорания топлива, а в низшую теплоту сгорания это количество теплоты не входит.
Водяные пары в дымовых газах образуются за счет испарения влаги самого топлива, при сгорании водорода, находящегося в топливе, и влаги, входящей в состав воздуха, который используют в качестве окислителя горючих компонентов топлива.
Теплота конденсации 1 кг водяного пара при атмосферном давлении составляет примерно 2500 кДж/кг. Количество водяных паров в рабочем топливе равно Wp/100. При сгорании 1 кг водорода получается 9 кг водяных паров (Н2 + 0,5О2 - Н2О). Следовательно, теплоту паров определяют из формулы:
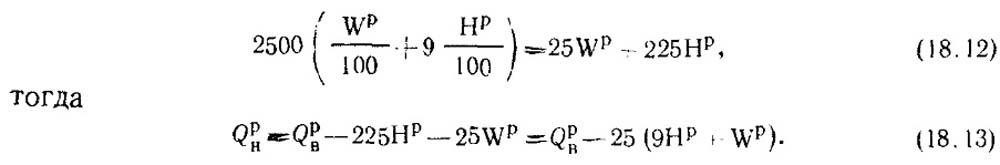
В лабораторных условиях теплоту сгорания твердого и тяжелого жидкого топлива (мазута) определяют с помощью калориметрической бомбы.
Схема калориметра показана на рис. 18.2. Калориметрическая бомба представляет собой стальной герметичный сосуд 1, заполненный кислородом под давлением 3 МПа. В сосуде сжигают навеску топлива в 1 г, отобранную из лабораторной пробы. Бомбу помещают в сосуд с водой 2 и по приращению температуры воды вследствие выделенной теплоты при сжигании навески топлива определяют теплоту его сгорания.
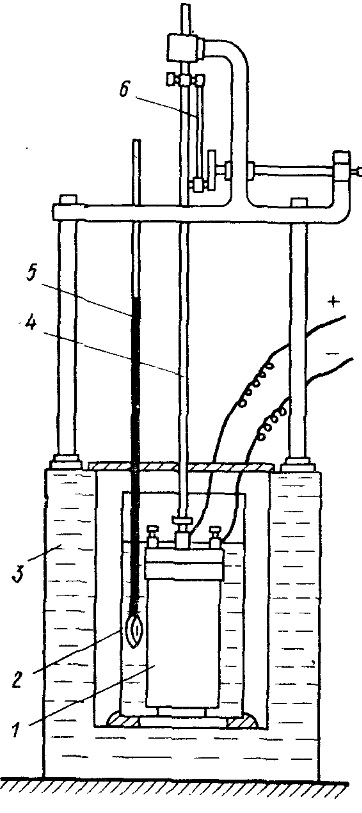
Рис. 18.2. Калориметрическая установка
1 - калориметрическая бомба; 2 - сосуд с водой; 3 - термостат; 4 - мешалка; 5 - термометр; 6 - приводной механизм мешалки.
Теплоту сгорания газообразного и легкого жидкого топлива (бензин, керосин и т. д.) определяют в калориметре Юнкерса, который представляет собой миниатюрный водогрейный котел, в топочном объеме которого сжигается топливо. Расход газа определяют по показанию счетчика, а расход жидкого топлива - весовым способом. Расход воды находят взвешиванием на весах или по измерительному сосуду. Зная разность температур воды при входе в калориметр и выходе из него, легко определяют теплоту, переданную воде. Затем по известному расходу газа или жидкого топлива подсчитывают теплоту его сгорания.
При известном элементарном составе твердого и жидкого топлив теплоту их сгорания, кДж/кг, можно приближенно определить по эмпирическим формулам, из которых наиболее распространена предложенная Д. И. Менделеевым:
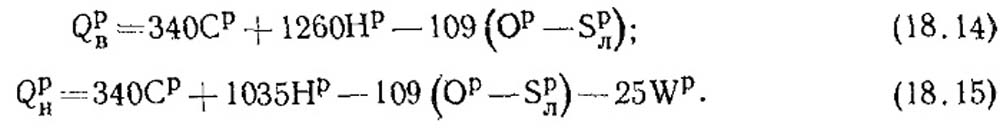
Теплоту сгорания сухого газа определяют по объемному составу, %, и известной теплоте сгорания компонентов.
Низшая теплота сгорания, кДж/м3, составит:
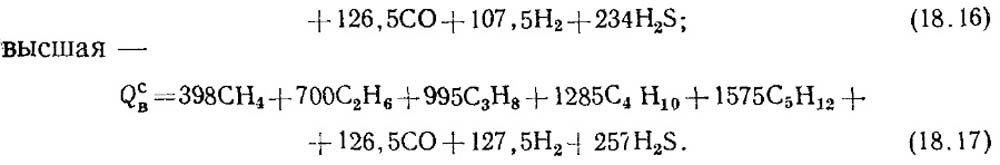
Величины Qс/н и Qс/в определяют по составу сухого газа.
Если в состав газа входят неизвестные углеводородные компоненты (при условий, что содержание метана известно), то сумму углеводородов условно принимают как содержание этана С2Н4 и теплоту сгорания рассчитывают по формулам, аналогичным уравнениям (18.16) и (18.17).
Теплоту сгорания природного газа можно также определять по углеродному числу n с помощью следующих линейных зависимостей, предложенных Г. Ф. Кнорре:
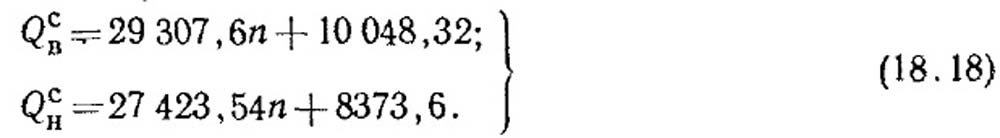
Теплота сгорания природного газа находится в пределах 33 000 - 36 000 кДж/м3, искусственных горючих газов - 3700 - 21 000 кДж/м3.
Для сравнения различных видов топлива по их тепловому эффекту и облегчения государственного планирования топливных ресурсов страны введено понятие об условном топливе, теплота сгорания которого принята равной 29 300 кДж/кг.
Отношение данного топлива к Q условного топлива называется топливным эквивалентом, обозначаемым буквой Э. Тогда для пересчета расхода натурального топлива Вн в условное Ву.т достаточно величину Вн умножить на эквивалент Э, т. е.
Ву.т = ВнЭ = ВнQр/нQу.т